科望医药ES014获FDA孤儿药资格 硬纤维瘤治疗迎来全球首创疗法新突破
2026年3月3日,科望医药正式宣布,其自主研发的全球首创CD39/TGF-β双特异性抗体ES014,获得美国食品药品监督管理局(FDA)授予的孤儿药资格认定,适应症为硬纤维瘤。这一里程碑式进展,不仅为全球硬纤维瘤患者带来了全新治疗希望,更为ES014的全球临床开发与商业化进程按下“加速键”。
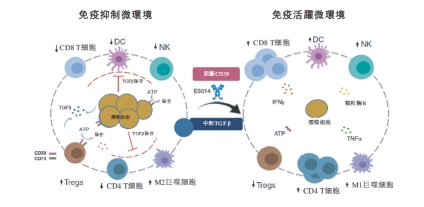
ES014作用机制
硬纤维瘤为罕见的局部侵袭性软组织瘤,可导致剧烈疼痛、身体功能受损及危及性命的并发症。目前的治疗方法通常会导致肿瘤复发或严重的副作用,患者对于更有效安全的疗法存在迫切需求。当前全球范围内仅一款药物获批专治硬纤维瘤,临床治疗存在巨大的未满足需求,尤其针对难治性、复发性患者,亟需安全有效的创新治疗方案。
ES014此次斩获FDA孤儿药资格,与其在临床研究中展现的积极数据表现密切相关。2025年12月,在欧洲肿瘤内科学会亚洲年会(ESMO Asia)优选论文专场,科望医药以口头报告形式公布了ES014的中国I期临床研究数据。研究结果显示,ES014显示出良好的安全性,未观察到剂量限制性毒性(DLT)且不良事件多为轻度。在5例可评估的硬纤维瘤患者中,ES014单药治疗实现了40%的客观缓解率(ORR),疾病控制率(DCR)更是达到100%;其中达到部分缓解(PR)的患者仍在持续接受治疗,展现出优异的疗效持续性,同时整体安全性可控,为这一罕见难治瘤种提供了极具潜力的创新治疗方向。
作为全球首个进入临床阶段的CD39/TGF-β双抗,ES014的创新机制为其临床价值奠定了坚实基础。硬纤维瘤的发生发展高度依赖β-catenin与TGF-β通路的协同驱动,同时肿瘤细胞高表达CD39。ES014初步成功挑战了行业面临的靶向TGF-抗肿瘤药物的研发难题,通过高亲和力靶向CD39,将强大的TGF-阻断作用“锚定”并限制在肿瘤微环境中CD39表达的免疫细胞和肿瘤细胞上,从而精准重塑抗肿瘤免疫力,同时避免对其他正常组织或肿瘤细胞产生非预期的影响。
此次FDA孤儿药资格认定,将为ES014带来多重政策红利,包括美国市场7年的市场独占期、临床试验相关费用的税费抵免、新药上市申请费用减免,以及FDA的临床开发专项指导支持,将大幅加速ES014全球的临床开发进程,推动这款中国原研创新药更快惠及全球患者。
近年来,科望医药持续深耕免疫疗法的源头创新,依托差异化技术平台布局多条具备全球竞争潜力的研发管线。ES014相继实现临床进展与国际监管的阶段性里程碑,持续验证了科望医药的原研创新实力。